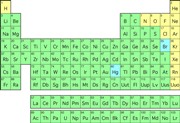
A nyilakkal válthatja az elektronpályák képeit.
 |
A nyilakkal válthatja az elektronpályák képeit. |
Hagyományosan a megfelelő pályákat, héjaknak hívják és betűkkel jelölik K, L, M, N, O, P, Q. Az egy héjon tartózkodó elektronok száma maximum 2n2 lehet.
Az első, az atommaghoz legközelebbi, K elektronpályán (1. sor) mindössze két s elektron "fér el". Ezek az atommagok központi nanocsövének irányában helyezkednek el, kétoldalt. (H-He)
A következő L héjon (2. sor) már összesen 8 (2s+6p) elektron tartózkodhat. A 2s elektron még tengelyirányú lehet, míg a 6p elektron egy hatos gyűrűt alkot, a magfelépítéshez hasonlóan. (Li-Ne)
A párhuzamos L héjon (3. sor) is összesen 8 (2s+6p) elektron tartózkodhat. A 2s elektron még tengelyirányú lehet, míg a 6p elektron szintén hatos gyűrűt alkot, a bipoláris elrendezés szerint. (Na-Ar)
Az ezt követő M héjon (4. sor) összesen 18 elektron lehetséges, de itt már az s pálya üres és a szerkezet (6p+12d), ami követi az atommag tóruszos felépülését. (K-Kr)
A párhuzamos M héjon (5. sor) is összesen 18 elektron lehetséges, az s pálya üres és a szerkezet (6p+12d) megfelel a bipoláris elektronhéj felépítésnek. (Rb-Xe)
A következő N héjon (6. sor) a számított 32 helyett összesen 36 elektron lenne lehetséges (6p+12d+18f), de a 6. sor s nélkül (6p+12d), követi a mag felépítését (a lantánnal együtt Cs-Rn).
A párhuzamos N héjon (7. sor) a 7. sor s nélkül (6p+12d), követi a mag bipoláris elektronhéj felépítését (az aktiniummal együtt Fr-Og).
A lantanidák (8. sor) az N héj 18f pályáit töltenék fel. Az aktinidák (9. sor) meg így az N héj 18f párhuzamos pályáit töltenék fel. Talán.
Az O héjon a hivatalos 2n2 számolás szerint 50 pálya lenne lehetséges, ha lenne ilyen héj. De az előbbiek alapján már nincs ilyen.
Az elektronok maximális száma így változik az egyes alhéjakon s2, p6, d12, és f18. Az s pálya csak a K és az L héjon van.
by H.Mika Electron shell ChatGPT discussion Gemini AI discussion